2024年11月24日,广东药科大学基础医学院李雄教授团队在British Journal of Cancer(JCR分区Q1,中科院医学1区,广药大共识期刊B刊)在线发表了题为SKP2 Inhibition Activates Tumor Cell-Intrinsic Immunity by Inducing DNA Replication Stress and Genomic Instability的研究论文。该论文首次报道了抑制E3连接酶SKP2增强三阴性乳腺癌(Triple-negative breast cancer, TNBC)抗肿瘤免疫应答的新机制。

TNBC是一种高侵袭性乳腺癌亚型,与其他亚型相比预后差,确诊5年内死亡率接近40%[1]。近年来以PD-1/PD-L1抗体为首的免疫检查点抑制剂(ICI)治疗多种癌症取得了较好临床效果,但对大多数转移性TNBC患者,疗效并不显著[2]。
ICI治疗效果与肿瘤微环境(tumor microenvironment,TME)中淋巴细胞的浸润密切相关。cGAS-STING作为细胞质内双链DNA主要的感应通路,在先天免疫反应和抗肿瘤免疫治疗中发挥重要作用。激活肿瘤细胞中的cGAS可以促进淋巴细胞浸润到TME中,从而提高ICI治疗效果[3]。SKP2 (S-phase kinase-associated protein 2)是SCF复合物中的E3连接酶蛋白,在乳腺癌中异常高表达,并促进恶性转化和癌症进展[4]。然而,SKP2是否调控TNBC的抗肿瘤免疫尚不清楚。
该研究首先用动物实验评价了抑制SKP2对TNBC移植瘤生长的影响。与免疫缺陷裸鼠的移植瘤相比,在免疫正常的BALB/c小鼠中抑制SKP2显示出了更强的肿瘤抑制效果,提示抑制SKP2可能激活了抗肿瘤免疫。的确,在免疫正常的BALB/c小鼠的移植瘤中,抑制SKP2后显著促进了肿瘤内淋巴细胞浸润,TME中CD8+T细胞比例明显升高。
该研究进一步揭示了抑制SKP2激活cGAS/STING通路的分子机理。除了CDT1,另一个DNA复制许可因子CDC6也是SKP2的底物。抑制SKP2同时升高了CDC6和CDT1的蛋白水平,引起DNA复制异常,增加DNA复制压力并损伤双链DNA,导致细胞基因组不稳定,从而增加胞质中的微核和DNA桥成分,激活cGAS/STING通路,促进了促炎细胞因子和趋化因子的分泌。动物实验也证实抑制SKP2显著激活了PD-1抗体的抗肿瘤免疫应答。
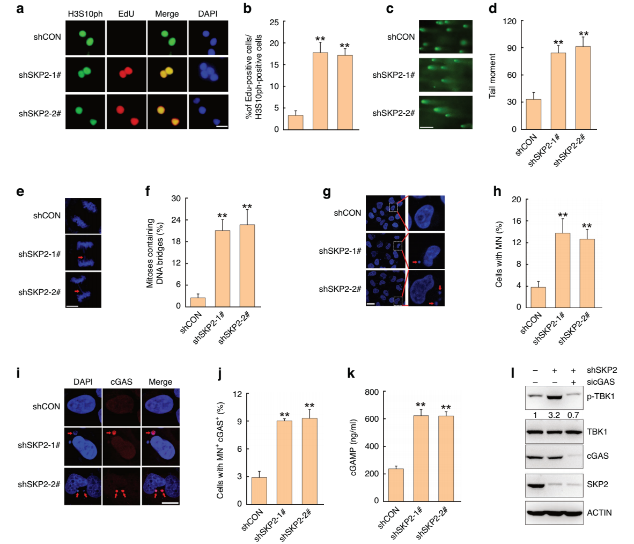
该研究揭示了在TNBC肿瘤细胞中抑制SKP2增强抗肿瘤免疫应答的分子机制,从而证明SKP2可作为有效的治疗靶点来增强ICI抗肿瘤免疫治疗的效果。
广东药科大学附属第一医院彭玉冲博士和广东药科大学基础医学院齐旭莉博士为该论文的共同第一作者,广东药科大学基础医学院李雄教授为通讯作者。该工作得到了国家自然科学基金、临床药学国家临床重点专科、广州市科技计划和广东药科大学学科培优重点团队项目等基金支持。
参考文献:
[1]Yin L, Duan JJ, Bian XW, Yu SC. Triple-negative breast cancer molecular subtyping and treatment progress. Breast Cancer Res 2020; 22: 61.
[2]Sanmamed MF, Chen L. A paradigm shift in cancer immunotherapy: From enhancement to normalization. Cell 2018; 175: 313–326.
[3]Li A, Yi M, Qin S, Song Y, Chu Q, Wu K. Activating cGAS-STING pathway for the optimal effect of cancer immunotherapy. J Hematol Oncol 2019; 12: 35.
[4]Cai Z, Moten A, Peng D, Hsu CC, Pan BS, Manne R et al. The skp2 pathway: A critical target for cancer therapy. Semin Cancer Biol 2020; 67: 16–33.